Подвижные молекулы препарата способствовали восстановлению спинного мозга у мышей
Нанофибрилы с веществами, способствующими восстановлению и выживанию клеток спинного мозга после его травмы, имеют лучшую эффективность, если сделать их молекулы подвижными.
Это показало исследование американских ученых, во время которого мыши с травмой спинного мозга лучше восстанавливались и возвращали себе двигательную функцию, если получали инъекцию нанофибрил с усиленной подвижностью их молекул. Результаты опубликованы в журнале Science. Травмы спинного мозга может привести к тяжелым последствиям, например, к параличу нескольких или всех конечностей. Часто эти последствия неотвратимы из-за низкой способность нервной системы к регенерации и образования рубцовой ткани, которая еще больше осложняет заживление. Пока нет такого лечения, которое с высокой эффективностью может восстановить двигательную функцию. Впрочем, исследования показывают, что отдельные химические вещества способны помочь. Например, хондроитиназа АВС растворяет глиальный рубец, препятствует восстановлению нервов. Другие ученые видят решение в соединениях, соответствующие рецепторы клеток активируют процессы регенерации. Естественно такими соединениями являются белки, но их фармакологическое использование ограничено коротким периодом дееспособности в человеческом организме после введения, а также высокой стоимостью изготовления.
Потенциально помочь могут искусственные материалы со свойствами внеклеточного матрикса, которые содержат более малые молекулы пептиды, имитирующие действие конкретных белков и, так же, связываясь с рецепторами клеток, могут активировать процессы заживления. При соединении их в большие плотные полимеры, они могут «жить» и действовать в организме гораздо дольше белков. Изучая такой подход к лечению травм спинного мозга, ученым из Северо-Западного университета и Исследовательской лаборатории ВВС США удалось добиться значительных успехов в опытах на животных.
Ученые создали супрамолекулярную структуру из полимеров, благодаря которой наноразмерные фибриллы удачно имитирует среду внеклеточного матрикса. Его терапевтическое действие обусловлено наличием двух типов пептидов в составе фибрилл. Первый IKVAV, содействует превращению нейрональных стволовых клеток в нейроны и удлинению аксонов — длинных отростков нейронов, которые, среди прочего, проводят сигналы к мышечным волокнам. Другой пептид называется YRSRKYSSWYVALKR, и он способствует разрастанию клеток и их выживанию.
Но чтобы эти вещества подействовали и запустили желаемые клеточные процессы, они должны связаться с соответствующими рецепторами на поверхности клеток. Это не так уж и просто, учитывая то, что рецепторы и другие структуры мембраны клеток находятся в движении и постоянно меняют свое расположение. Чтобы помочь взаимодействию пептидов с рецепторами, ученые модифицировали не биоактивные участки фибрилл таким образом, чтобы сделать их более подвижными. Благодаря этому молекулы, как и рецепторы, постоянно находятся в движении.
Препарат лучше всего применять в виде инъекции. При введении он образует гелиевую структуру с нанофибриламы. В таком виде он может в течение нескольких недель находиться и действовать в организме. Испытания средства провели на мышах через 24 часа после тяжелого повреждения спинного мозга, которое проявилось параличом нижней части тела, в частности конечностей, животных. Эффективность препарата сравнивали с действием инъекции обычного солевого раствора.
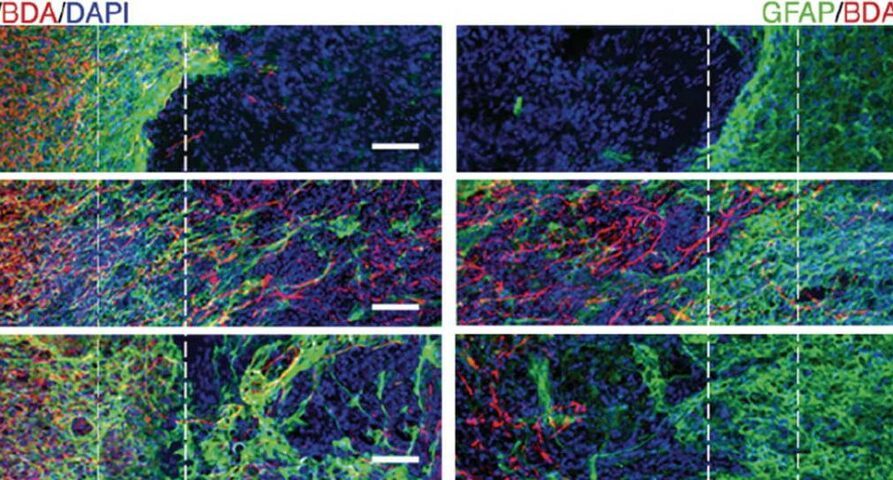
За 12 недель наблюдения у мышей, которым ввели солевой раствор, почти не обнаружили восстановления аксонов. Зато в группе лечения комбинированным препаратом восстановления аксонов было в 50 раз больше, а кроме этого наблюдалось усиленное покрытие аксонов миелином — изолирующим белком, который обеспечивает быструю и корректную передачу электрических сигналов. Терапия также проявилась существенно меньшей плотностью глиального рубца в месте повреждения, по сравнению с мышами первой группы. У мышей второй группы после инъекции препарата за три месяца на месте повреждения образовалась новая сеть кровеносных сосудов, по сравнению с мышами после укола солевого раствора. У этих сосудов наблюдалась большее количество нейронов, в частности мотонейронов; картина была подобна как у здоровых животных с неповрежденным спинным мозгом. Это указывает на то, что лечение действительно помогло повысить выживаемость нейронов. Изменения от лечения были заметны и в поведении животных. Уже через три недели после поражения животные продемонстрировали лучшие показатели, частично восстановив двигательную функцию, в частности возможность ходить.
Поэтому ученые провели опыты в пробирках с человеческими клетками сосудов и клетками-предшественниками нейронов. Опыты снова показали, что пептиды в составе фибрилл способны запустить необходимые для заживления спинного мозга клеточные процессы.
Что интересно, наибольшая терапевтическая эффективность (восстановление аксонов и кровеносных сосудов, функциональное улучшение) наблюдалось при применении фибрилл из самых подвижных молекул. Ученые считают это доводом в пользу того, что постоянная смена формы фибрилл в результате их сильно подвижных молекул способствует лучшему взаимодействию с рецепторами. Но не исключено, что динамическая сеть фибрилл влияет на клетки опосредованно, лучше взаимодействуя с белками внеклеточного матрикса. Ученые надеются, что их открытие может помочь лечению и других заболеваний.
Ученым не первые удается вернуть возможность ходить мышам с травмой спинного мозга. В начале года вышло исследование, где подобных успехов удалось достичь благодаря инструментам генной терапии.
Перевод материала nauka.ua